Propaani
Propaani:n tärkeydestä on keskusteltu vuosikymmeniä. Olipa kyseessä henkilökohtainen, ammatillinen tai akateeminen, Propaani:llä on ratkaiseva rooli jokapäiväisessä elämässämme. Propaani on ollut eri alojen asiantuntijoiden tutkimuksen ja tutkimuksen kohteena Propaani:n alkuperästä sen nykyiseen kehitykseen. Tässä artikkelissa tutkimme Propaani:n eri puolia sen vaikutuksesta yhteiskuntaan sen merkitykseen historiassa. Lisäksi analysoimme, kuinka Propaani on vaikuttanut ja muokannut elämämme eri puolia ja tarjoaa syvemmän käsityksen sen merkityksestä nykymaailmassa.
| Propaani | |
|---|---|
 |
|
 |
|
| Tunnisteet | |
| Muut nimet | n-Propaani |
| CAS-numero | 74-98-6 |
| PubChem CID | 6334 |
| Ominaisuudet | |
| Molekyylikaava | C3H8 |
| Moolimassa | 44,1 g/mol |
| Ulkomuoto | väritön kaasu |
| Sulamispiste | −187,6 °C (85,5 K) |
| Kiehumispiste | −42,09 °C (231,1 K) |
| Tiheys | 0,0018324 g/cm3 (kaasu, 25 °C, 1 atm)[1] |
| Liukoisuus veteen | 0,007 g / 100 ml (20 °C) |
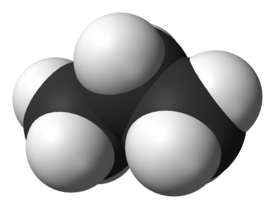
Propaani eli n-propaani (C3H8), jonka rakennekaava on CH3CH2CH3, on normaaliolosuhteissa väritön, hajuton ja tulenarka kaasu. Se on suoraketjuinen alkaani, jonka moolimassa on 44,1 g/mol, sulamispiste −189,7 °C, kiehumispiste −42,1 °C, leimahduspiste −104 °C, itsesyttymislämpötila 450 °C ja CAS-numero 74-98-6.
Propaania erotetaan tislaamalla maaöljystä tai -kaasusta. Sitä käytetään muun muassa kotitalouksissa ja teollisuudessa nestekaasuna seoksena butaanin kanssa sekä joissakin spraymaaleissa.[3] Kilogramma propaania sisältää energiaa 12,8 kWh (46 MJ). Propaanista valmistetaan myös lukuisia yhdisteitä, kuten eteeniä, propeenia, propanolia, isopropanolia ja propanaalia. Myös propaanin klooratut johdannaiset ovat merkittäviä teollisuuskemikaaleja.[4]
Turun yliopiston biokemian laitoksella on onnistuttu tuottamaan propaania Escherichia coli -bakteerin avulla. Tämä on ensimmäinen tunnettu propaania tuottava biosynteesimenetelmä.[5]
Propaanin elintarvikkeiden E-koodi on E944. Elintarvikkeissa propaania käytetään lähinnä ponneaineena[6] tai pakkauskaasuna.
Palaminen
Propaanin palaessa syntyy hiilidioksidia (CO2) ja vettä (H2O).
- C3H8 + 5 O2 → 3 CO2 + 4 H2O
Käyttö päihtymystarkoituksessa
Propaania käytetään joskus päihdetarkoituksessa imppaamalla.[3]
Lähteet
- ↑ Susan Budavari (päätoim.): The Merck Index, s. 1341. (12th Edition) Merck & Co., 1996. ISBN 978-0-911910-12-4 (englanniksi)
- ↑ Propaani Käyttöturvallisuustiedote. 30.12.2015. Sigma-Aldrich (Merck). Viitattu 5.3.2021.
- ↑ a b Imppaus Päihdelinkki.fi. 9.6.2014. Viitattu 15.5.2021.
- ↑ Alén, Raimo: Kokoelma orgaanisia yhdisteitä: Ominaisuudet ja käyttökohteet, s. 19. Helsinki: Consalen Consulting, 2009. ISBN 978-952-92-5627-3
- ↑ Mikrobit saatiin tuottamaan propaania 3.9.2014. Turun yliopisto. Viitattu 5.3.2021.
- ↑ E944 - Propaani Ruokavirasto. Viitattu 26.9.2023.
Aiheesta muualla
- Propaanin kansainvälinen kemikaalikortti
- Pauli Kallio, András Pásztor, Kati Thiel, M. Kalim Akhtar & Patrik R. Jones: An engineered pathway for the biosynthesis of renewable propane, Nature Communications 5, Article number: 4731, Published 02 September 2014 (englanniksi)
- PubChem: Propane (englanniksi)
- Human Metabolome Database (HMDB): Propane (englanniksi)
- Kyoto Encyclopedia of Genes and Genomes (KEGG): Propane (englanniksi)
| Alkaanit | {| style="text-align:center;" |
| width="70px" | metaani | width="70px" | etaani | width="70px" | propaani | width="70px" | butaani | width="70px" | pentaani | width="70px" | heksaani | width="70px" | heptaani | width="70px" | oktaani | width="70px" | nonaani | width="70px" | dekaani | width="70px" | undekaani | width="70px" | dodekaani |- | CH4 | C2H6 | C3H8 | C4H10 | C5H12 | C6H14 | C7H16 | C8H18 | C9H20 | C10H22 | C11H24 | C12H26 |- |} |
|---|---|
| Alkeenit | {| style="text-align:center;" |
| width="70px" | | width="70px" | eteeni | width="70px" | propeeni | width="70px" | buteeni | width="70px" | penteeni | width="70px" | hekseeni | width="70px" | hepteeni | width="70px" | okteeni | width="70px" | noneeni | width="70px" | dekeeni | width="70px" | undekeeni | width="70px" | dodekeeni |- | | C2H4 | C3H6 | C4H8 | C5H10 | C6H12 | C7H14 | C8H16 | C9H18 | C10H20 | C11H22 | C12H24 |- |} |
| Alkyynit | {| style="text-align:center;" |
| width="70px" | | width="70px" | etyyni | width="70px" | propyyni | width="70px" | butyyni | width="70px" | pentyyni | width="70px" | heksyyni | width="70px" | heptyyni | width="70px" | oktyyni | width="70px" | nonyyni | width="70px" | dekyyni | width="70px" | undekyyni | width="70px" | dodekyyni |- | | C2H2 | C3H4 | C4H6 | C5H8 | C6H10 | C7H12 | C8H14 | C9H16 | C10H18 | C11H20 | C12H22 |- |} |
argon (E 398) | butaani (E 943a) | happi (E 948) | helium (E 939) | hiilidioksidi (E 290) | isobutaani (E 943b) | propaani (E 944) | typpi (E 941) | typpimonoksidi (E 942) | vety (E 949)

