Rasvahappoamidihydrolaasi
Tässä artikkelissa aiomme tutkia Rasvahappoamidihydrolaasi:tä ja sen merkitystä nykyisessä kontekstissa. Rasvahappoamidihydrolaasi on ollut keskustelun ja tutkimuksen kohteena useilla eri aloilla, ja se on kiinnostava aihe alan tutkijoille, ammattilaisille ja asiantuntijoille. Vuosien varrella Rasvahappoamidihydrolaasi on osoittanut merkittävän vaikutuksen jokapäiväisen elämän eri osa-alueisiin, sen vaikutuksista yhteiskuntaan ja rooliin uusien teknologioiden kehittämisessä. Tämän artikkelin avulla pyrimme analysoimaan ja ymmärtämään Rasvahappoamidihydrolaasi:n tärkeyttä sekä sen vaikutuksia eri tietoalueisiin.
| Rasvahappoamidihydrolaasi | |
| |
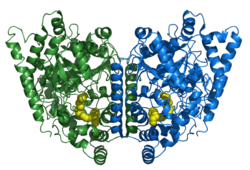
| Rotan FAAH:n homodimeeri (PDBID: 1MT5). Aktiivisissa kohdissa on arakidonihapon inhibiittoreina toimivat johdannaiset (keltaisella). | |
| Tunnisteet | |
| EC-numero | 3.5.1.99 |
| Tietokannat | |
| KEGGt | KEGG |
| Entrez | 2166 |
| OMIM | 602935 |
| UniProt | O00519 |
Rasvahappoamidihydrolaasi eli FAAH on nisäkkäiden lipidikalvoista löytyvä entsyymi (amidaasi), joka hajottaa hydrolyysin kautta joitakin rasvahappojen amideita. Se hajottaa eritoten anandamidia arakidonihapoksi ja 2-aminoetanoliksi sekä vähäisessä määrin 2-arakidonyyliglyserolia arakidonihapoksi ja glyseroliksi. 2-AG:tä hajottaa ensijaisesti monoasyyliglyserolilipaasi eli MAGL. Anandamidi ja 2-AG ovat tärkeimmät nisäkkäiden endokannabinoidit. FAAH hydrolysoi keskeisesti myös endokannabinoideihin kuulumattomia N-palmitoyylietanoliamiinia (PEA) ja oleyylietanoliamiinia (OEA), jotka vähentävät tulehdusreaktioita ja kiputuntemuksia.[1]
Ihmisillä on myös rasvahappoamidihydrolaasi 2 (FAAH2), joka on eri entsyymi kuin FAAH. FAAH2 on kuitenkin toiminnoiltaan samankaltainen kuin FAAH.[2]
Geeni, rakenne ja sijainti
Ihmisillä FAAH:n geeni on FAAH ja se on kromosomissa 1 kohdassa 1p33.[3] Ihmisten FAAH koostuu yhdestä 579:n aminohapon peptidiketjusta, jonka massa on noin 60 kDa. Solukalvoissa se on homodimeeri.[4]
FAAH:ta on ihmisillä paljon eritoten keskushermostossa, joissa se on lähinnä soomassa ja tuojahaarakkeissa solujen sisäisissä kalvoissa, kuten sileässä solulimakalvostossa ja mitokondrioiden ulkokalvoissa. Sitä on myös muualla kehossa, mutta alueellisesti keskushermostoa rajoittuneemmin.[1]
Lääkinnällinen merkitys
FAAH:n toimintaa estäviä aineita voitaisiin käyttää kipu- tai masennuslääkkeinä, sillä esto lisää kannabinoidireseptoreihin aktivoivasti sitoutuvien endokannabinoidien pitoisuuksia ihmiskehossa. Estäjät voisivat siis toimia vaihtoehtona tetrahydrokannabinolin kaltaisille ulkoisille kannabinoidireseptorien agonistien annostelulle.[1]
FAAH-estäjiä on kehitetty monia, mutta mitään niistä ei ole toistaiseksi hyväksytty lääkemarkkinoille. Useat FAAH-estäjät ovat osoittautuneet vaarattomiksi, mutta joidenkin estäjien testaus on lopetettu esimerkiksi siksi, että niiden on havaittu olevan lääkinnällisesti tehottomia. Kuitenkin vuonna 2016 Bial-lääkeyhtiön kehittämän "BIA 10-2474"-nimisen kokeellisen FAAH-estäjän antaminen Ranskassa 90:lle koehenkilölle johti yhden koehenkilön kuolemaan aivoverenvuodon takia ja aiheutti neljälle pysyvän aivovaurion.[5]
Puutos
Vuonna 2019 tuolloin 66-vuotiaalta skotlantilaiselta naiselta löydettiin toimimaton FAAH:n geeni yhdestä alleelista (eli heterotsygoottinen puuttuvan toiminnan mutaatio). Alleelista oli poistunut pieni osa eli kyse oli mikrodeleetiosta. Mutaation seurauksena muodostuneelle toimimattomalle geenille eli pseudogeenille annettiin nimi FAAH-OUT. Mutaation takia nainen ei ollut tuntenut elämänsä aikana koskaan kipua (katso kongenitaalinen analgesia), pelkoa tai ahdistusta, mutta poti huonomuistisuutta. Mutaation takia naisella oli veressään noin 70% normaalia enemmän anandamidia sekä noin kolme kertaa enemmän oleyylietanoliamiinia ja palmitoyylietanoliamidia.[6]
Lähteet
- ↑ a b c K Ahn, DS Johnson, BF Cravatt: Fatty acid amide hydrolase as a potential therapeutic target for the treatment of pain and CNS disorders. Expert opinion on drug discovery, 2009, 4. vsk, nro 7, s. 763–784. PubMed:20544003 doi:10.1517/17460440903018857 ISSN 1746-0441 Artikkelin verkkoversio.
- ↑ S Sirrs et al: Defects in fatty acid amide hydrolase 2 in a male with neurologic and psychiatric symptoms. Orphanet Journal of Rare Diseases, 2015, 10. vsk. PubMed:25885783 doi:10.1186/s13023-015-0248-3 ISSN 1750-1172 Artikkelin verkkoversio.
- ↑ JA López-Moreno, V Echeverry-Alzate, K Bühler: The genetic basis of the endocannabinoid system and drug addiction in humans. Journal of Psychopharmacology, 2012, 26. vsk, nro 1, s. 133–143. PubMed:21937688 doi:10.1177/0269881111416689 ISSN 1461-7285 Artikkelin verkkoversio.
- ↑ M Lorca et al: Three-dimensional quantitative structure-activity relationships (3D-QSAR) on a series of piperazine-carboxamides fatty acid amide hydrolase (FAAH) inhibitors as a useful tool for the design of new cannabinoid ligands. International Journal of Molecular Sciences, 2019, 20. vsk, nro 10, s. 2510. PubMed:31117309 doi:10.3390/ijms20102510 Artikkelin verkkoversio.
- ↑ R Kaur, P Sidhu, S Singh: What failed BIA 10–2474 phase I clinical trial? Global speculations and recommendations for future Phase I trials. Journal of Pharmacology & Pharmacotherapeutics, 2016, 7. vsk, nro 3, s. 120–126. PubMed:27651707 doi:10.4103/0976-500X.189661 ISSN 0976-500X Artikkelin verkkoversio.
- ↑ AM Habib et al: Microdeletion in a FAAH pseudogene identified in a patient with high anandamide concentrations and pain insensitivity. British Journal of Anaesthesia, 2019, 123. vsk, nro 2, s. e249–e253. PubMed:30929760 doi:10.1016/j.bja.2019.02.019 ISSN 0007-0912 Artikkelin verkkoversio.